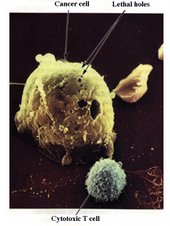
CANCER-VIRUS SU RELACION
23
REVISIONES BIBLIOGRAFICAS
FACULTAD DE CIENCIAS MEDICAS
PROVINCIA GUANTANAMO.
CANCER Y VIRUS.
Dr. Ibrahim Ganén Prats1 , Dra. Madelaine Aguilar Peláez 2 .
1 Especialista de I Grado en Bioquímica Clínica. Profesor Instructor del Departamento de Fisiología.
2Especialista de I Grado en Pediatría. Hospital General Docente “Dr. Agostinho Neto”
INTRODUCCION
Cada día se da más importancia al
tema de la relación entre los virus y
el cáncer, tanto en el aspecto
patogénico como en la genética
molecular.
La proliferación y diferenciación
celular es un proceso cuidadosamente
regulado que responde a las
necesidades específicas del organismo.
En un organismo joven la
multiplicación celular supera la
muerte celular y así el organismo
aumenta de tamaño; en un adulto, el
proceso de regeneración y muerte
celular está equilibrado en forma de
un estado estacionario. Algunos
tipos de células, como los
eritrocitos humanos, viven aproximadamente
120 días y, sin embargo,
las células intestinales tienen
pocos días de vida media, por lo que
las células intestinales deben ser
sustituidas casi inmediatamente, lo
que no ocurre con los eritrocitos.
Los mecanismos que regulan la
multiplicación celular fallan y
entonces las células comienzan a
crecer y dividirse incontrolablemente,
el resultado es un clon
de células que termina formando una
masa celular denominada tumor.
La formación de este tumor
obedece a cambios en el material
genético (DNA) de las células
somáticas. Entre estos cambios, la
alteración de genes preexistentes a
oncogenes es el más importante. Los
productos de los oncogenes son los
causantes del crecimiento celular
inapropiado, por lo que queda claro
que la alteración del DNA parece
24
ser la clave de la inducción del
cáncer.
Entre los agentes causantes de la
alteración de los genes preexistentes
a oncogenes se encuentran
los virus, tanto DNA como
RNA. Un grupo de virus RNA, los
retrovirus, y muchos tipos de virus
DNA pueden favorecer la
transformación; a estos virus se les
denomina virus tumorales.
Dado que estos virus han desarrollado
la capacidad de transformación
de diferentes maneras,
consideraremos estas dos clases de
virus tumorales por separado.
DESARROLLO
Los virus DNA tienen un genoma
que puede contener de 5 hasta 200
kb, por lo que sus genomas pueden
ser lo mismo pequeños que mayores.
Aunque todos los virus DNA pueden
ser virus tumorales, comenzaremos
con los papovavirus, de los cuales los
más conocidos y representativos son
el SV40 (B.K. en humano) y el virus
del polioma (J.C. en humano).
Estos virus inducen en las células
infectadas el paso de la fase Go ó
G1 a la fase S, por lo que la fase
temprana de la infección se produce,
y se replica tanto en DNA
celular como el vírico en algunas
células animales denominadas células
permisivas; a esta fase temprana le
sigue una fase tardía o de síntesis
masiva del virus y muerte de las
células. Por lo que cada papovavirus
tienen sus células permisivas;
mientras las células de ratón son las
permisivas para el virus del polioma,
para el SV40 lo son las células de
mono.
En algunos tipos de células
denominadas no permisivas hay
conexión de la fase tardía de la
infección con la fase temprana, y
entonces las células continúan el
ciclo celular y se convierten en
células permanentemente transformadas
(cancerígenas). En ocasiones,
el virus no puede pasar a la fase
tardía de infección y la céluala
puede transformar en no permisiva.
Al parecer, el DNA de los papovavirus
no se integra en un punto
específico del DNA celular, sino que
parece ser que se integra al azar.
Los productos o proteínas víricas
pudieran ser los causantes de
mantener el estado cancerígeno de
las células. Por lo dicho hasta ahora,
la asociación entre el cáncer y los
virus parece estar relacionado con
la presencia de genes transformantes
en el genoma viral, la incorporación
al DNA celular y la no
llegada de la célula a la fase tardía.
Lo anterior da lugar a proteínas
transformantes codificadas por los
virus, y que son la causa de la
25
transformación cancerígena. En los
momentos actuales, el virus de
Epstein-Barr (virus DNA) constituye,
al parecer, la causa primaria
del linfoma de Burkitt y de algunos
tumores nasofaríngeos, donde se
han encontrado el antígeno característico
del virus de Epstein-Barr.
Existen, además, estudios que
plantean una alta relación enttre el
cáncer de hígado y el virus de la
hepatitis B (virus DNA), ya que
alrededor del 60% de los pacientes
con cáncer de hígado presentan
antígenos para el virus de la
hepatitis B.
Un grupo de virus RNA, los
retrovirus, pueden ser agentes
transformantes; a estos virus se les
denomina también virus tumorales.
Recordemos que los retrovirus
fienen dos moléculas de RNA (8500
nucleótidos), y cada una se une a un
TRNA, a lo que hay que añadir que
cada virión contiene transcriptasa
inversa (es capaz de copiar RNA a
DNA). Una vez en el citoplasma, la
transcriptasa inversa forma un DNA
de doble hebra que es copia de la
información genómica del RNA
vírico, y más grande que el mismo,
ya que tiene a ambos extremos una
repetición terminal larga, que dirige
la integración del DNA de doble
hebra en un sitio específico del
cromosoma celular. Una vez en el
DNA celular, el DNA de doble hebra
(DNA provírico) se convierte en el
molde para la síntesis de RNA. Este
RNA vírico sirve como mRNA para
la síntesis de proteínas víricas
(proteínas transformantes) y como
RNA.
La capacidad transformante del
retrovirus no está en su genoma
básico sino en el material genético
que adquiere del DNA celular
normal. Es por eso que los retrovirus
son virus transductores que tienen
capacidad para transducir oncogenes,
o genes que inducen cáncer.
Esta capacidad transuctora de los
retrovirus permite que genes
normales en algunos animales, al ser
adquiridos por estos virus, se
comporten como oncogenes. Esto
lleva a la consi-deración de que la
información genética celular puede
ser la causante de la inducción
tumoral y deja claro que nuestros
propios genomas contienen genes
que pueden, en ciertas circunstancias,
causar cáncer.
El virus de la leucemia del gato
pertenece al grupo de los virus
oncógenos del ARN, que se encuentran
ampliamente diseminados en la
naturaleza. Ellos provocan la
leucemia en muchos tipos de
mamíferos, y además sarcomas y
tumores en ratones y primates.
26
CONSIDERACIONES
Aun cuando faltan evidencias de la
relación entre el cáncer y los virus,
queda claro que éstos son importantes
y a tener en cuenta en la
etio-logía del cáncer. Entre los
virus relacionados con cánceres
humanos están los siguientes:
carcinomas nasofaríngeos, producidos
por el virus de Epstein-
Barr, leucemia de las células T
humanas (virus de la leucemia de las
células T humanas(HTLV), cáncer
del hígado (virus de la hepatitis B) y
el carcinoma cervical humano (virus
del papiloma humano).
CUADRO COMPARATIVO. VIRUS TUMORALES RNA Y DNA.
VIRUS RNA VIRUS DNA
Integración al ADN
celular
En sitio específico Al azar
Tamaño del genoma
viral
8500 nucleótidos cada
molécula
5-200 kb
Ciclo vital Una vez integrado
dirige la síntesis de
nuevas progenies
víricas
Una vez integrado puede
provocar la lisis celular
Transducción de genes Sí No
Virus oncógenos Virus HTLV Virus Epstein-Barr, virus
de la Hepatitis B, virus
del papiloma
Localización de la
capacidad transformante
Genoma básico de la
célula normal
Genoma básico del virus
BIBLIOGRAFIA
1. Alfaro M, Molina S. Displasias uterinas relacionadas con diversos agentes infecciosos. Rev Méd Costa
Rica. 1994; (61):7-9.
2. Chabner B A. Oncología. En: Wyngaarden J B. Smith L H, Bennett J C. Tratado de Medicina Interna
19 de. T 1, México: Interamericana 1992: 1186-1187.
27
3. De la Torre Díaz A, Rosales Elorduy F, Mora Tiscareño A, Ramírez Gaytán J L, Frías Mendivil M.
Correlación entre variables ginecobstétricas con lesiones morfológicas por virus del papiloma humano.
Rev Inst Nac del Cáncer de México 1994; (4): 76-80.
4. Derchan S F, Andrade L A, Silva L C. Risk factors for uterine condiloma in sexually active adolescent
women. Rev Asoc Méd de Brasil 1972; (41):130-134.
5. Espinar A C. Cáncer. En: Piédrola Gil G, Domínguez C M, Cortina Grens P, Gálvez Vargas R, Sierra López
A, Sáenz González M C. Medicina Preventiva y Salud Pública 8a. ed. Barcelona: Salvat; 1990:723-726,
6. Fernández C, Sharrard R M, Talbot M, Reed B D, Monks N. Evaluation of the significance of
polyamines and their oxidases in the etiology of human cervical carcinoma. Ed Br J Cáncer 1995;
(5):1194-1199.
7. Guyton A C. Eritrocitos, anemia, policitemia. Tratado de Fisiología Médica. T 1, La Habana: Editorial
Revolucionaria, 1990: 47-48.
8. Giraldo G E. Role of viruses in human cancer. Elsevier 1984: 175-179.
9. Kanno T Brown K, Franzoso G, Siebenlist V. Kinetic Analysis of Human T-Cell Leukemia Virus Type I
Tax- Mediated Activation of NF-KB . En: Molecular and Cellular Biology. USA De Board
1994;(14):6443-6451.
10. Mattheus R F. Classification and nomenclature of viruses: Third of the International Committee on
Taxonomy of viruses. Intervirology 1989; (9):129-130.
11. Morphy W P, Lawrence W, Lenhard R E. Oncología Clínica, Manual de la American Cancer Society.
OPS 1996, 9:194-5.
12. Melnick L. Viruses, Oncogenes and cancer. New York: S Kancer 1985; (2):123-127.
13. Oliveira da Silva, A D, De Albuguergue L A, Chaib E, Saad W A, Pinotti H E. Small Hepatocellular
carcinoma: new concepts apropos of the intrahepatic recurrence after hepatectomy in the
orthotropic liver transplantation. Rev Asoc Med de Brasil 1995; (42):15-18.
14. Overturf K, Al-Dhalimy M, Tanguary R, Brantly M, Ou C. N, Finegold M. Hepatocytes corrected by
gene therapy are selected in vivo in a murine model of hereditary type I. De Nat Genet USA 1996;
(3):232-233.
15. Propst A, Propst T, Waldenberger P, Judmare G, Vogel W. Hepatocellular Carcinoma. De Klinik fur
Innere Medizin 1995; (44):2137-2142.
16. Rein R. Molecular Basis of Cancer, part A: Macro-Mole-Structure, Carcinogenes and Oncogenes,
1985; (1):134-137.
17. Reif A E: The causes of Cancer. American Science 1981:456-458.
18. Rein R. Biolecular Basis of Cancer, part B: Micro-Mole-Recognition, Chemotherapy, and Immunology
1985; (2):1122-1124.
19. Reif A C. The Causes of Cancer: American Science 1981:455.
28
20. Sears R, Sealy L. Multiple forms of C/EBP Bind the EFII Enhancer Sequence in the Rous Sarcoma
Virus Long Terminal Repeat. En: Molecular and Cellular Biology. USA Ed. Board, 1994; (14):4855-
4877.
21. U pton A C. Principios de la biología del cáncer: etiología y prevención del cáncer. En: Devita V T,
Helman S, Rosenberg S A. Cáncer. Principios y prácticas de Oncología T 1, La Habana: Editorial
Científico Técnica; 1985:36-38.